Feu vert au premier traitement
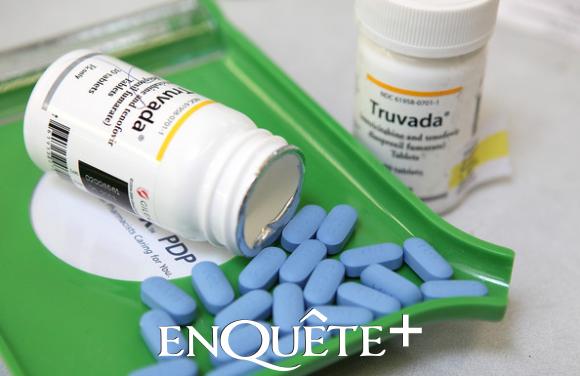
La FDA, l'agence américaine des médicaments, a donné son feu vert lundi à la mise sur le marché de l'antirétroviral Truvada, premier traitement de prévention contre le sida.
Suivant une recommandation d'un comité d'experts, la Food and Drug Administration a approuvé le Truvada, du laboratoire américain Gilead Sciences, "afin de réduire le risque de transmission du virus du sida (VIH) à des sujets sains à haut risque d'être contaminés", a précisé l'agence dans un communiqué.
Le Truvada est destiné "à être utilisé à titre prophylactique avant un contact avec le VIH (virus de l'immunodéficience humaine), en combinaison avec des pratiques sexuelles sûres comme l'usage de préservatifs et d'autres mesures de prévention --dépistage régulier et traitement d'autres maladies vénériennes-- pour empêcher la transmission du virus chez des adultes à haut risque", a souligné l'agence.
"Le Truvada ne peut pas se substituer à des pratiques sexuelles sûres", selon le communiqué. L'efficacité préventive du Truvada a été mise en évidence par les résultats d'un essai clinique mené de juillet 2007 à décembre 2009 dans six pays, dont le Brésil, l'Afrique du Sud et les Etats-Unis, et financé en grande partie par les Instituts nationaux américains de la santé (NIH). Il avait alors réduit de 44% le risque d'infection chez les hommes homosexuels qui utilisaient aussi un préservatif.
Une autre étude clinique a montré que le Truvada a diminué le risque d'infection jusqu'à 75% chez les couples hétérosexuels dont l'un des deux partenaires était séropositif.
7sur7

























